产品详情
往20mL硫酸和盐酸的混合溶液中,加入0.05mol/LBa(OH)2溶液时,生成BaSO4的量和溶液的pH变化如图.试回答:
(1)起始时,混酸中H2SO4的物质的量浓度为多少?
(2)起始时,混酸中盐酸的物质的量浓度为多少?
(3)B点时溶液的pH是多少?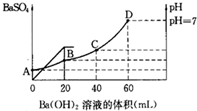
试题答案
由图可知,0~20mLBa(OH)2溶液发生H2SO4+Ba(OH)2═BaSO4↓+H2O,20mL~60mLBa(OH)2溶液发生发生H++OH-═H2O,

(1)设硫酸的物质的量为x,则H
2SO
4+Ba(OH)
2═BaSO
4↓+H
2O 1 1 x 0.02L×0.05mol?L
-1=
,解得x=0.001mol,硫酸的物质的量浓度为
=0.05mol?L
-1,答:起始时,混酸中H
2SO
4的物质的量浓度为0.05mol/L;(2)设HCl的物质的量为y,则H
++OH
-═H
2O1 1y 0.04L×2×0.05mol/Ly=0.002mol,则盐酸的浓度为
=0.2mol/L,答:起始时,混酸中盐酸的物质的量浓度为0.2mol/L;(3)由图可知,B点硫酸完全反应,氢离子的浓度为
| 0.2mol/L×0.02L |
| 0.02L+0.02L |
=0.1mol/L,所以pH=1,答:B点时溶液的pH是1.



