下列离子方程式表达正确的是

A.漂白粉溶液中通入过量的CO2:ClO-+CO2+H2O=HClO+HCO3-
B.碳酸钠水溶液呈碱性的原因:CO32-+2H2O 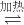 H2CO3+2OH-
H2CO3+2OH-
C.向溴化亚铁溶液中通足量氯气:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl-
D.向稀硫酸中加入少量Ba(OH)2溶液:H++SO42-+Ba2++OH-=BaSO4↓+H2O
试题答案
A
试题解析
A、过量二氧化碳与次氯酸钙反应生成碳酸氢钙和次氯酸;
B、碳酸根离子是多远弱酸阴离子分步水解;
C、溶液中离子还原性为Fe2+>Br->Cl-,过量氯气把亚铁离子和溴离子全部氧化,离子方程式中量少的符合化学式的组成比;
D、酸碱中和反应生成硫酸钡沉淀和水配平化学方程式得到;
解答:A、漂白粉溶液中通入过量的CO2,反应的离子方程式为:ClO-+CO2+H2O=HClO+HCO3-;故A正确;
B、碳酸钠水溶液呈碱性的原因是因为碳酸根离子水解:CO32-+H2O=HCO3-+OH-;故B错误;
C、向溴化亚铁溶液中通足量氯气,溶液中离子还原性为Fe2+>Br->Cl-,过量氯气把亚铁离子和溴离子全部氧化,离子方程式中量少的符合化学式的组成比;反应的离子方程式为:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl-;故C错误;
D、向稀硫酸中加入少量Ba(OH)2溶液,反应的离子方程式为:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,故D错误;
故选A.
点评:本题考查离子反应方程式的书写,明确发生的化学反应是解答本题的关键,注意常与量有关的离子反应即可解答,选项D为易错点,题目难度中等.

